
摘要:根据国家疾控中心相关的尼帕病毒实验室检测技术方案,旨在提供Pipetty电动移液器在尼帕病毒实时荧光定量RT-PCR检测中的具体应用,结合核酸提取、RT-PCR反应体系配制、扩增检测等核心实验环节,发挥其精准微量移液、高效操作、防交叉污染的优势,规范实验操作步骤,保障尼帕病毒核酸检测结果的准确性、重复性和可靠性,为实验室开展尼帕病毒快速筛查与确诊提供标准化技术支撑。
方案详情:
一、实验原理
尼帕病毒属于单股负链RNA病毒,实时荧光定量RT-PCR(Realtime RT-PCR)技术是检测该病毒的核心方法,其原理是先通过反转录酶将病毒RNA逆转录为cDNA,再以cDNA为模板,利用尼帕病毒特异性上游引物、下游引物与荧光探针,在Taq酶作用下进行PCR扩增。扩增过程中,荧光探针与目的片段特异性结合,随着扩增循环的进行,荧光信号不断累积,通过仪器实时监测荧光强度,可实现对尼帕病毒核酸的定性判断和定量分析。

二、实验准备
1、设配和材料
① Pipetty电动移液器MSIC01-03-20,MSIC01-03-250;
② 核酸提取仪;
③ PCR扩增仪;
④ 生物安全柜;
⑤ 水浴锅;
⑥ 冰箱和冰柜;
⑦ 离心机。
2、试剂和材料
① 上游引物TCA-GCA-GGA-AGG-CAA-GAG-AGT-AA;
下游引物CCC-CTT-CAT-CGA-TAT-CTT-GAT-CA;
荧光探针FAM-CCT-CCA-ATG-AGC-ACA-CCT-CCT-GCA-G-TAMRA;
② RT-PCR试剂盒;
③ 阴性对照;
④ 阳性对照;
⑤ 无核酶水;
⑥ RNA提取试剂。
三、实验步骤
1、将待测样本(如血液、脑脊液、尿液等)在生物安全柜中进行预处理。
2、反应条件根据实验室具体使用的商业化 Realtime RT-PCR试剂盒为准,以QIAGEN公司OneStepRT-PCR试剂盒为例。核酸扩增检测的反应体系如下:
3、反应体系
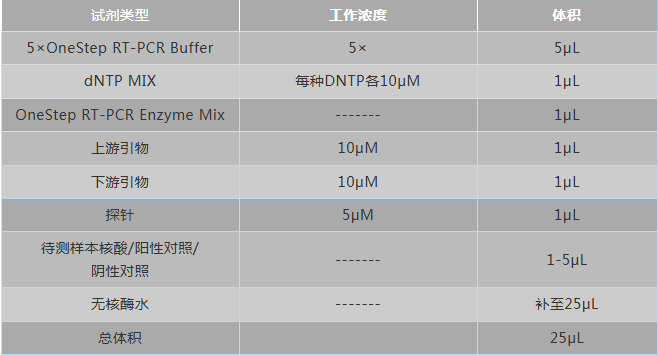
注:每次检测均需配制阳性对照和阴性对照作为实验室检测质控。
4、使用Pipetty电动移液器根据预设的荧光PCR反应体系表,设置单次分液模式;先计算所需总孔数,将除待测样本之外的所有试剂按对应体积计算后,额外增加10%的试剂体积,精准移取至同一离心管中,开启移液器混匀模式,将试剂自动混匀。
5、将Pipetty电动移液器切换至连续分液模式,根据单孔反应体系体积,精准吸取混合好的试剂,分别加入到96孔PCR板的对应孔中。再用移液器精准吸取对应体积的待测样本,加入到对应孔中,将96孔板放入高速离心机,离心。
6、反应程序设置(按照实时荧光定量PCR扩增仪说明书操作):
反转录阶段:50℃,30分钟;95℃,15分钟(无循环,完成反转录及酶激活);
扩增阶段:95℃,30秒(变性);55℃,30秒(退火);72℃,60秒(延伸),读取荧光信号,共40个循环;
扩增结束后,仪器自动生成扩增曲线和Ct值,用于结果判定。

四、结果判定
1、尼帕病毒核酸实时荧光定量RT-PCR 方法实验室检测有效性判读条件:
(1)阳性对照Ct值<35;
(2)阴性对照无Ct值(无扩增曲线)。同时满足上述两个条件,实验室检测结果有效;上述任一条件不满足,实验室检测结果无效。
2、待测标本核酸实验室检测结果判读:
(1)待测标本Ct值<35,标本为尼帕病毒阳性;
(2)待测标本Ct值>38,标本为尼帕病毒阴性;
(3)待测标本Ct值≥35且Ct值≤38,标本需要再次提取核酸进行复核检测。